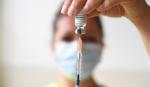
Dự kiến dùng vaccine dịch tả lợn châu Phi trên cả nước vào tháng 2-2023
Bộ Nông nghiệp và Phát triển nông thôn cho biết, trong tháng 2 tới đây, vaccine dịch tả lợn châu Phi dự kiến sẽ được sử dụng trên phạm vi cả nước.
 |
| Trong tháng 2-2023, vaccine dịch tả lợn châu Phi sẽ được sử dụng trên toàn quốc. Ảnh: Thành Hoa |
Tại cuộc họp về giám sát chất lượng việc sử dụng 600.000 liều vaccine AVAC ASF LIVE của Công ty CP AVAC Việt Nam diễn ra vào hôm nay (31-1), Bộ Nông nghiệp và Phát triển nông thôn cho biết, dự kiến trong tháng 2 tới đây, vaccine dịch tả lợn châu Phi sẽ được sử dụng trên toàn quốc.
Bộ yêu cầu Công ty CP AVAC Việt Nam tiếp tục theo dõi và đánh giá độ miễn dịch của vaccine sau khi tiêm, giám sát virus ngoài thực địa, bổ sung thêm một số chỉ tiêu đánh giá liên quan như việc tiêu tốn thức ăn.
Vaccine phòng bệnh dịch tả lợn châu Phi AVAC ASF LIVE do Công ty CP AVAC Việt Nam nghiên cứu, sản xuất và được cấp phép lưu hành vào tháng 7-2022. Vaccine được đưa vào sử dụng có giám sát tại các trang trại chăn nuôi heo. Số lượng là 10 lô vaccine với 600.000 liều.
Tính đến cuối tháng 12-2022, đơn vị đã tiêm trên 1.800 con heo. Kết quả, tỷ lệ miễn dịch đạt 94,4%. Ngoài ra, sau 14 ngày tiêm vaccine, số lượng đàn heo này có kháng thể 40% và đạt 90% sau 28 ngày tiêm vaccine. Đến tháng 1-2023, 4 lô vaccine của công ty đã được kiểm nghiệm và đạt yêu cầu đối với các chỉ tiêu đề ra.
Ngoài ra, năm 2022, Việt Nam là nước đầu tiên nghiên cứu, sản xuất thành công hai sản phẩm vaccine dùng cho việc phòng bệnh dịch tả lợn châu Phi. Đó là vaccine NAVET-ASFVAC của Công ty CP thuốc thú y Trung ương Navetco và vaccine AVAC ASF LIVE của Công ty CP AVAC Việt Nam.
Dự kiến, đầu năm 2023, Bộ Nông nghiệp và Phát triển nông thôn sẽ đánh giá việc sử dụng 1,2 triệu liều vaccine phòng bệnh dịch tả lợn châu Phi của hai công ty trên và quyết định đưa vào sử dụng trên phạm vi toàn quốc.
(Theo thesaigontimes.vn)
 về đầu trang
về đầu trang